
锂离子电解液溶剂/空气混合物爆炸特性实验研究
据能源圈了解到,
摘 要 本工作利用爆炸极限与点火能测试反应平台开展了典型锂离子电解液溶剂碳酸甲乙酯(EMC)蒸气爆炸实验,首次测量了不同初始温度与当量比条件下EMC的最大爆炸压力Pmax、爆炸下限LFL等爆炸危险性基础参数,并利用数值模拟方法开展了燃烧化学反应动力学机理分析数值模拟分析。结果表明EMC/空气混合气体的最大爆炸压力Pmax随着当量比的增加呈先增大后减小的趋势,并且在当量比图片=1.2附近取到最大值;随着温度的增加,Pmax呈递减的趋势,且Pmax与初始温度的倒数1/T0呈线性关系;由于存在热损失,在相同工况下,Pmax,exp均小于最大绝热爆炸压力Pmax,ad。EMC/空气混合气体的爆炸下限LFL随着T0的升高而降低,并呈线性关系,且对燃料爆炸下限经典模型的参数进行了修正,修正后的新公式的预测值与实验值结果吻合较好;通过反应机理分析得到不同T0对于LFL的影响方式主要是通过影响OH⋅自由基的生成速率来实现的。本研究可为定量评估EMC的爆炸危险性提供一定依据以及为其实际使用中制定相应的安全标准提供一定参考。
关键词 碳酸甲乙酯;最大爆炸压力;爆炸下限;初始温度;当量比
《新能源汽车产业发展规划(2021—2035 年)》明确指出:发展新能源汽车是我国从汽车大国迈向汽车强国的必由之路,也是应对气候变化、推动绿色发展的战略举措。数据显示,2023年我国新能源汽车累计销售量为949.5万辆,已占据汽车市场份额的31.6%。其中,电动汽车因其环保、经济、易保养等特点,成为新能源汽车发展的主要推动力量。
随着电动汽车数量的增加,因锂离子电池热失控而引发的电动汽车火灾事故不断发生。事故原因调查结果显示电池问题是造成新能源汽车火灾事故的最大根源,有效防治新能源汽车火灾爆炸事故,应该重点关注锂电池性能以及着火物质。作为电动汽车的核心部件,锂离子电池的正极材料(如锂钴氧化物、锂铁磷酸盐等)和电解液都是易燃物质,一旦电池因过充放、短路、物理碰撞或高温等原因发生热失控,这些易燃物质会迅速燃烧,加剧火势。尽管锂电池电解液的质量仅仅占锂电池总质量的14%,但是其燃烧释放的热量可以占锂电池燃烧总释放热量的50%左右,有机烷基碳酸酯常作为电解质在锂电池中被广泛应用,选择烷基碳酸盐是因为它们对锂离子电池阴极和阳极稳定性影响较小,在冰点和沸点之间温度范围合理,具有良好导电性、低毒性,以及较好的安全特性。实际的电解液是由含有低黏度溶剂,如碳酸二甲酯(DMC)、碳酸二乙酯(DEC)以及不对称的碳酸甲乙酯(EMC)的混合物组成,以增加电解质的电导率。近年来,上述3种典型线性碳酸酯被大量应用于锂离子电池电解液中,有效地拓宽了锂离子电池的工作范围。相较于DMC和DEC,EMC在面对阴极、锂金属及石墨化合物时更加稳定。然而碳酸酯的大量使用,带来了不容忽视的火灾安全问题。近年来,已有多起碳酸酯相关的火灾事故被报道。比如:2023年5月11日,广东嘉拓新能源科技有限公司东莞分公司发生一起包含EMC在内的电解液火灾,过火面积约4000平方米,导致3人死亡,直接经济损失为792.17万元。2021年4月16日,北京市丰台区锂电池储能电站施工调试过程中起火,造成3人死亡,1人受伤,直接财产损失1660.81万元。鉴于上述情况,对EMC的燃烧爆炸特性进行深入研究显得尤为迫切,尤其是锂电池在热失控条件下会产生不同程度的高温,这对电解液的爆炸行为具有重要的影响,因此相关研究亟待加强。
1999年,Kumai等对一个轻微过充的商用18650电池进行了气体分析研究,在环境温度25 ℃,多次循环后不发生电池结构破裂的情况下,电解液中的DMC和EMC均出现了挥发并在锂电池外被检测到。研究锂离子电池安全性的学者们采用量热仪对EMC的应用及火灾安全进行了研究。Chen等采用锥形量热仪对包括EMC在内的4种常见碳酸盐溶剂及其混合溶液的燃烧性能进行了测试,主要对不同热辐射条件下溶液的热释放速率、质量损失率和总热释放速率进行分析,发现线性碳酸盐通常在锂电池燃烧过程的早期发生燃烧。Eshetu等基于火焰传播量热仪对EMC及其混合物的闪点、点火难易度、放热率、有效燃烧热、质量损失率以及火灾毒性进行了研究。
在燃烧反应模型方面,EMC的研究起步较晚。2022年,Takahashi等才提出了首个包含EMC化学动力学的机理模型。之后,Grgoire等在常压条件下利用反射激波管与一氧化碳光谱诊断研究了DMC、DEC和EMC的热解机制,反应温度范围为1230~2375 K。Zhang等采用喷射搅拌反应器和气相色谱实验研究了DMC、DEC和EMC的热解和高当量比氧化特性。这些研究中,EMC通常与DMC和DEC共同被研究,提出的机理也包含3种酯类的子反应集合。Takahashi等和Grgoire等均在文章中提及,EMC的燃烧爆炸特性实验值缺乏。
本工作旨在通过开展EMC/空气混合气体爆炸实验,获取EMC在不同初始温度以及当量比工况下的最大爆炸压力Pmax、爆炸下限(lower explosion limit, LFL)等基础爆炸特征数据,为定量评估EMC的爆炸危险性提供一定依据,以及为其实际使用中制定相应的安全标准提供一定参考,并且还可为验证EMC机理准确性与可靠性提供重要参数。
1 实验与理论研究方法
1.1 实验研究平台
图1是本工作采用的爆炸极限与点火能测试反应平台结构示意图,整个平台是基于ASTM E681:04《化学品(蒸气和气体)易燃性浓度限值的标准试验方法》设计的。该平台由以下几个重要部分构成,分别是爆炸容器、进样系统、加热系统、点火系统、数据采集系统以及集成式综合控制系统。
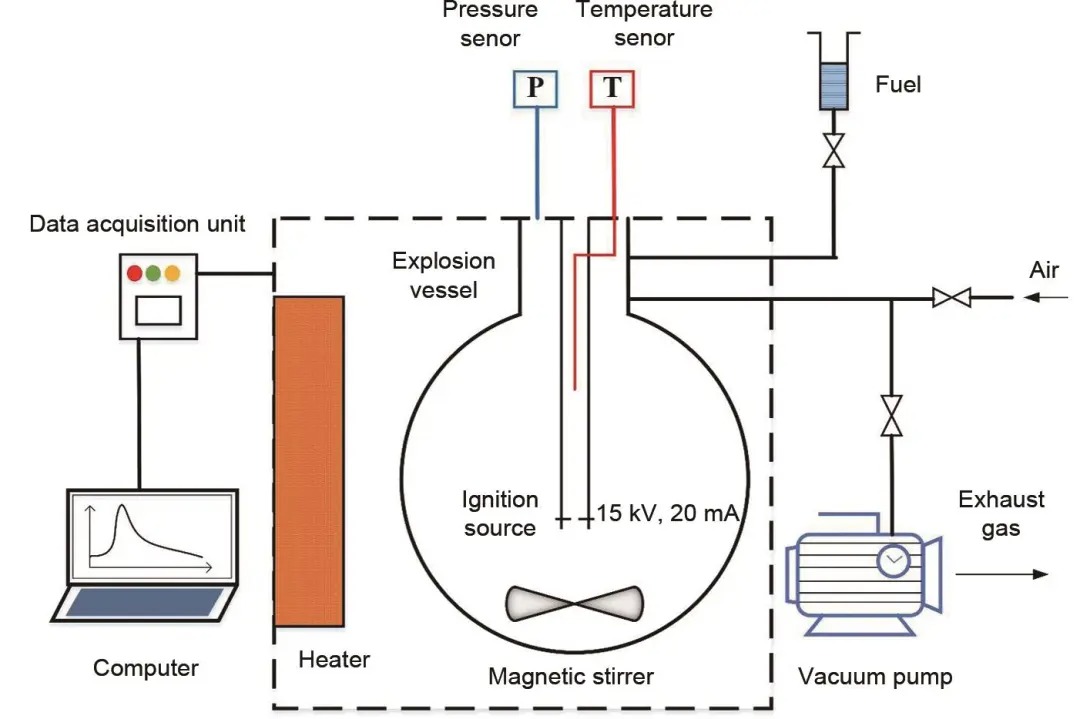
图1 实验设备平台示意图
平台主体为一个5 L的由S31603不锈钢制成的球形爆炸容器,容器的最大耐冲击压力为4 MPa,在容器底部有一个采用耐高温高压材料制成的磁力搅拌系统,其工作温度范围为-80~ 350 ℃,搅拌速度为0~450 r/min。容器上部则与爆炸泄压口以及进样系统相连,泄压口通过一个手动泄压阀与容器主体相连。进样系统由4个部分组成,分别是配气压力表(压力范围为0~110 kPa)、四条气体进样管路、一条液体进样管路以及真空泵,其采用分压法精密比例配气,分辨率为0.01 kPa。加热系统则主要由加热控制器(双路PID智能恒温控制)、空气温度传感器(位于爆炸容器与外部箱体之间,测温范围为0~200 ℃,分辨率为0.1 ℃)、爆炸容器内部温度传感器(测温范围为0~1350 ℃,分辨率0.1 ℃)以及红外加热器构成。点火系统则分为2部分,一部分为内置的450 J脉冲点火器(脉冲电压为15 kV,电流为30 mA;点火电极间距为2~8 mm;点火时间为1~1000 ms);另一部分为外置的连续脉冲点火器(电火花能量为0.1~1000 mJ,分辨率为0.1 mJ,能量递增梯度为0.1~10.0 mJ)。数据采集系统由专门的爆炸压力传感器(压力检测范围为0~2 MPa,分辨率为0.1 kPa)以及数据采集卡(采样间隔为0.2 ms,采样时间为0~5 s)构成。集成式综合控制系统则通过计算机内的设备操作软件控制其余各个系统的运行工作,包括抽真空、加热、点火、搅拌以及数据采集等,同时在操作界面会实时显示容器内部的压力与温度数据。
1.2 实验操作步骤
实验中使用的EMC纯度≥99.99%,由合肥市金品仪器设备有限公司提供。
(1)插上电源,启动实验设备,进行手动操作检验容器气密性,确保爆炸容器抽完真空后压力上升速率小于0.1 kPa/min;打开电脑设备控制软件,设定实验所需的压力与温度条件,启动加热系统,将容器内部升温至实验目标温度。
(2)在等待加热过程中,配置今日所需的液体燃料,通过小型针筒注入到设备上部的液体进样容器中,并用塑封膜做好密封工作;待加热到设定温度后,打开真空泵进行抽真空,使其压力低于0.6 kPa。
(3)打开进液管路阀门,根据事先计算好的燃料浓度进行进样,在达到预设浓度后关闭阀门,打开进气管路阀门,补入空气,使容器内部压力达到步骤(1)中所设压力值。
(4)开启磁力搅拌器300 s,以确保燃料蒸气和空气混合均匀;触发点火系统,点火时间设定为200 ms,点火后等待数据采集系统获取压力与温度数据。
(5)数据传输完成后,手动打开泄压阀,排出容器内部超压气体后关闭泄压阀,再次启动真空泵对容器进行抽真空,使其压力降至2 kPa以下,随后重新充入空气进行清洗,该步骤重复3次。对数据进行简单预处理,根据BSEN 1839:2017,若压力数据上升幅度超过设定压力的5%,则认定爆炸发生,该组数据保留,同种工况下每个实验至少重复3次,根据BS EN 15967:2011,每次实验测得的最大爆炸压力偏差如果不超过50 kPa,则认为该组数据有效。
1.3 球形火焰数值模拟
本工作中采用的EMC机理,是由Takahashi等构建的首个EMC机理。Takahashi等采用了Nakamura等的DEC机理作为基础,添加了EMC相关的反应。之后,又进一步添加了来自于Alexandrino等的DMC机理中的DMC相关反应。从仅有的EMC热解理论计算文献及实验测量文献中,Takahashi等获得了EMC分解反应的速率常数。但在该机理的构建过程中,还有一部分速率常数来源于对DMC和EMC机理中类似基元反应的估计。最终形成的详细机理共包含371个组分,2076个反应。
2 实验结果与分析
2.1 当量比对EMC/空气最大爆炸压力的影响
根据电池日常使用环境以及EMC的沸点等热物性参数,实验与模拟研究中初始温度T0选取了300 K、320 K、340 K、360 K和380 K共5个温度点;初始压力固定为常压即100 kPa;当量比图片选取跨度在0.6~1.4之间,间隔为0.1。
图2显示了不同温度以及不同当量比条件下实验所测得的最大爆炸压力值Pmax,exp以及模拟所计算得到的最大绝热爆炸压力Pmax,ad随当量比变化情况,每个工况至少重复3次,实验误差由图中黑色误差棒表示。可以看出,同种工况下Pmax,ad的值都高于Pmax,exp的值,这是由于实验系统并不是理想绝热系统,其爆炸所产生的能量只有部分用于系统内部温度与压力的提高,还有一部分能量则会被容器壁吸收;随着当量比的增加,实验所得Pmax,exp以及模拟的Pmax,ad都呈现出先增大后减小的趋势,均在当量比图片附近取到最大值,分别为753.03 kPa与992.02 kPa。然而随着温度的增加,不管是实验值Pmax,exp还是模拟值Pmax,ad则都呈现出下降的趋势,在当量比为0.6的条件下,300 K时实验值Pmax,exp为596.47 kPa,而在同当量比时,各温度下的Pmax,exp和Pmax,ad均随温度的升高而降低。由理想气体方程可知,在固定压力以及容器体积的条件下,温度越高,初始混合气体的量就越少,从而其最终爆炸的能量也会减少,从而降低了实验与模拟的Pmax值。
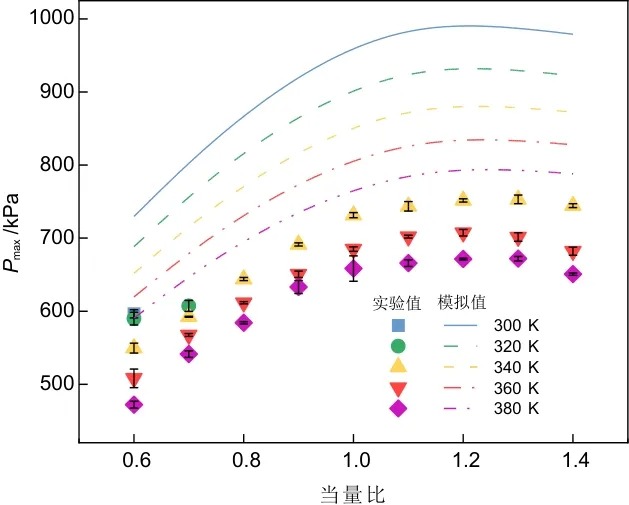
图2 不同初始温度下实验最大爆炸压力Pmax,exp和模拟计算所得最大爆炸压力Pmax,ad随当量比的变化
为进一步探究当量比对不同温度工况下的最大爆炸压力的影响规律,根据郑康雪的研究采用三阶多项式的方法把相关数据点进行拟合,得到的相关曲线如下:

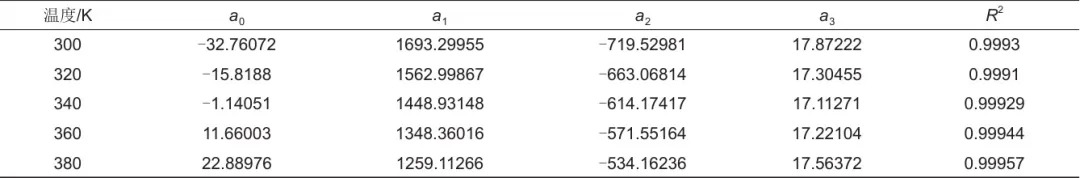
表1 实验最大所得爆炸压力Pmax,exp随当量比变化的拟合系数

表2 模拟计算所得最大爆炸压力Pmax,ad随当量比变化的拟合系数
2.2 初始温度对EMC/空气最大爆炸压力的影响

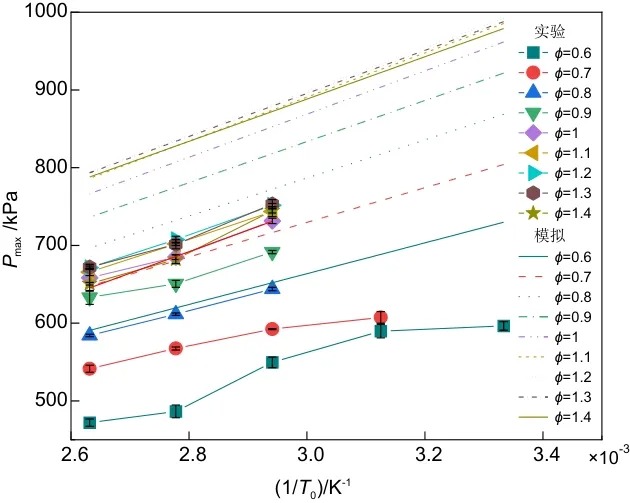
图3 不同当量比下最大爆炸压力Pmax随初始温度倒数1/T0的变化
为了进一步探究温度对于不同当量比工况下的最大爆炸压力的影响规律,以Razus等提出的最大爆炸压力与初始压力以及初始温度相关性公式为基础,进行变形后可获得最大爆炸压力与初始温度倒数1/T0的关系式,变形后的公式如下:


表3 实验所得最大爆炸压力Pmax,exp随温度倒数1/T0变化的拟合系数
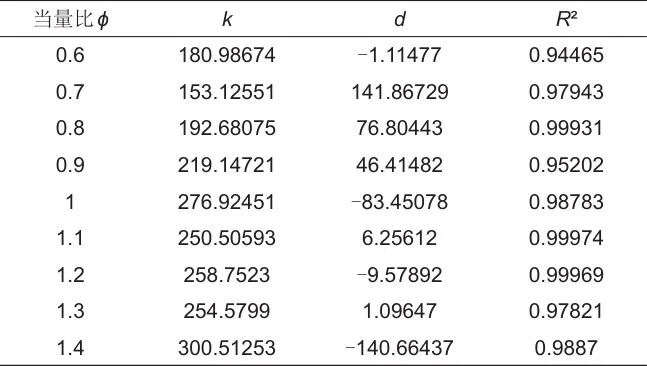
表4 最大绝热爆炸压力Pmax,ad随温度倒数1/T0变化的拟合系数
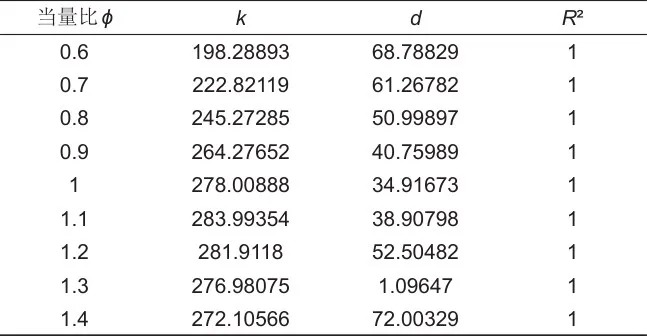
可以看出不管是Pmax,exp还是Pmax,ad,两者拟合曲线的R2都超过了0.94,且根据表4中斜率的变化规律,能很好地证明式(4)与式(5)中关于直线斜率k表达式的正确性,通过该拟合直线可很好地定量预测某一当量比下不同温度的EMC/空气的爆炸危险性。
2.3 初始温度对EMC/空气爆炸下限的影响
Zabetakis与Coward等发现了绝热火焰温度与初始温度之间的关系,建立了不同初始温度下燃料爆炸下限LFL预测的模型:

Chemkin-Pro对EMC机理的3个文件进行前处理后可获取反应中各个组分随温度变化的热物性数据,可在Mechanism Parameters处查看,数据显示EMC的图片在300~380 K之间变化非常小,取其在340 K时的606.7 kJ/mol作为公式代入值,由于不同温度下爆炸下限的变化值相对于混合气总体量来说也是非常小的,因此可认为混合物的总比热容保持不变,取0.0315 kJ/(mol⋅℃)作为公式代入值,修正系数α取为0.8。
如图4所示,实验值用实心点表示,预测值用虚线值表示,两者都随着初始温度的升高而降低,变化范围从300 K工况下的2.53%至380 K工况下的2.22%。因为初始温度的升高会增加混合物分子当中的内能,活化分子数量增多且运动剧烈,分子间的有效碰撞次数增加,从而使得反应更容易发生。并且由式(6)分析可知,EMC爆炸下限随温度的变化规律应是呈线性的,图中也很好地反映了这一点;图4(b)显示了EMC爆炸下限实验值与预测值之间的对比,可以发现EMC的实验值与预测值都分布在斜线y=x附近,证明预测结果非常好,与实验结果很相近;图4(c)显示了EMC爆炸下限实验值与预测值的相对误差,因为预测是以340 K工况条件下的爆炸下限作为预测基准,所以其相对误差为0,而其他温度工况条件下其相对误差绝对值的最大值仅为0.89%,说明式(7)能够很好地预测不同初始温度工况条件下的EMC爆炸下限。
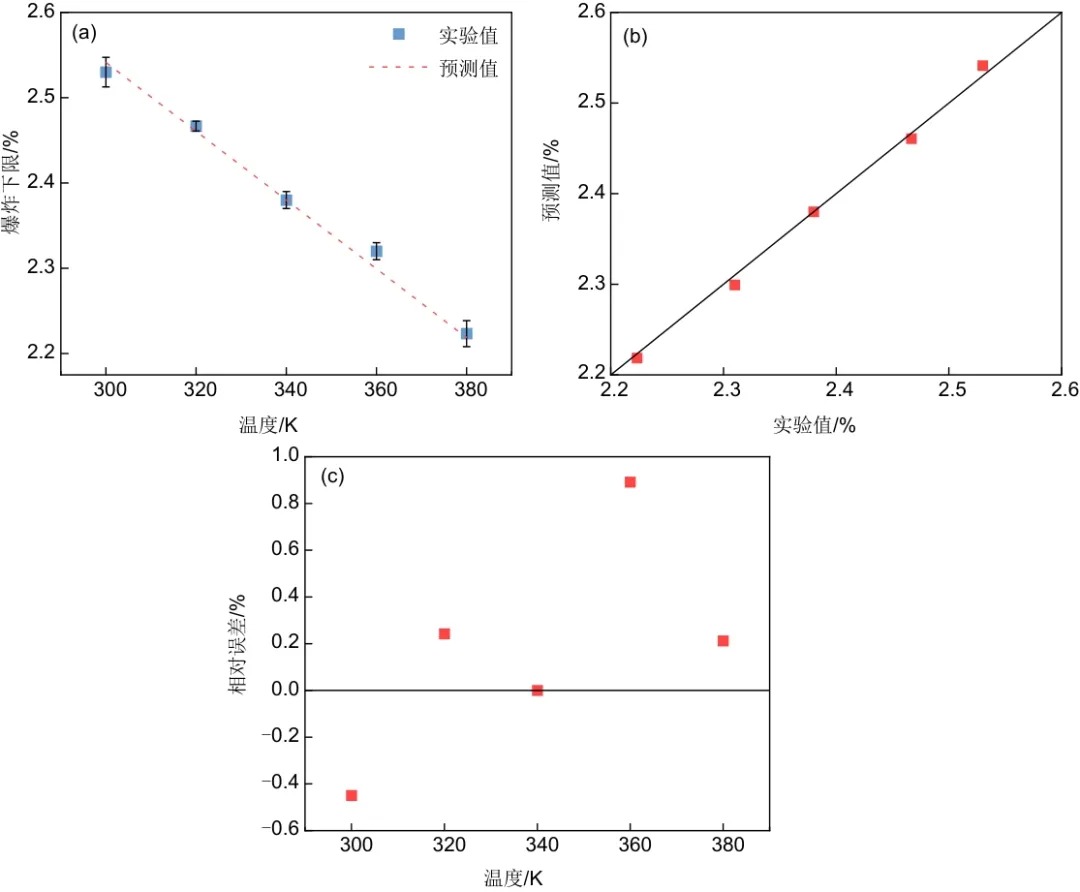
图4 (a) EMC爆炸下限随温度的变化;(b) 爆炸下限实验值与预测值的对比;(c) 爆炸下限实验值与预测值的相对误差
为进一步探究温度对于爆炸下限的影响方式,通过Chemkin-Pro中的预混层流预混燃烧模型对层流燃烧速度(LBV)进行敏感性分析。图5显示了不同初始温度下EMC爆炸下限浓度的LBV归一化敏感系数。可以发现随着初始温度的升高,不同反应的敏感性系数普遍呈增大的趋势。增强反应活性的基元反应主要是H⋅+O2=O⋅+OH、CO+OH=CO2+H⋅和HCO+M=H⋅+CO+M,降低反应活性的基元反应主要有H⋅+O2(+M)=HO2(+M)和HO2+OH⋅=H2O+O2,起到正向促进LBV作用的反应是H⋅、O⋅、OH⋅这三类自由基的主要来源,而消耗这三类自由基的反应则会对LBV起到抑制作用,这表明H⋅、O⋅、OH⋅这三类自由基是基元反应中产生和消耗的最重要的自由基,因此,应进一步研究反应过程中H⋅、O⋅、OH⋅自由基的摩尔分数变化情况。
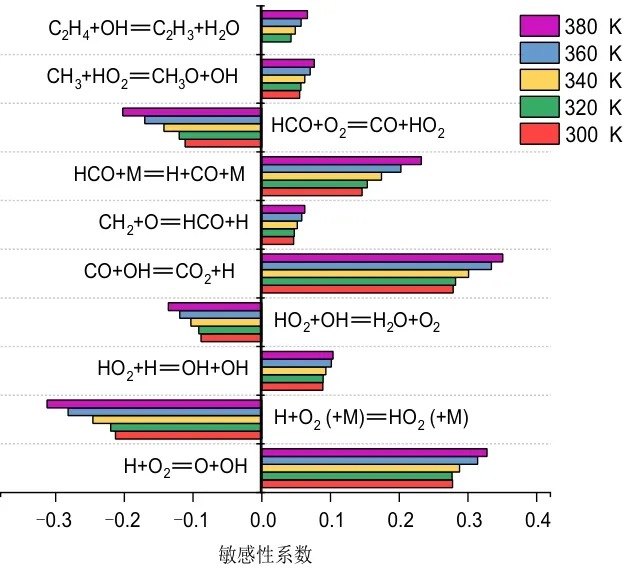
图5 初始温度对EMC爆炸下限浓度下层流燃烧速度归一化敏感系数的影响
图6显示了不同初始温度下EMC的爆炸下限工况下H⋅、O⋅和OH⋅自由基的摩尔分数。H⋅、O⋅、OH⋅自由基的峰值摩尔分数随着初始温度的增加而持续下降,并最终趋向于0。相较于H⋅、O⋅自由基峰值变化幅度,OH⋅自由基的变化幅度较大,OH⋅自由基峰值摩尔分数的降低意味着反应物难以维持燃烧,这与爆炸下限随着初始温度的升高而降低的规律一致。
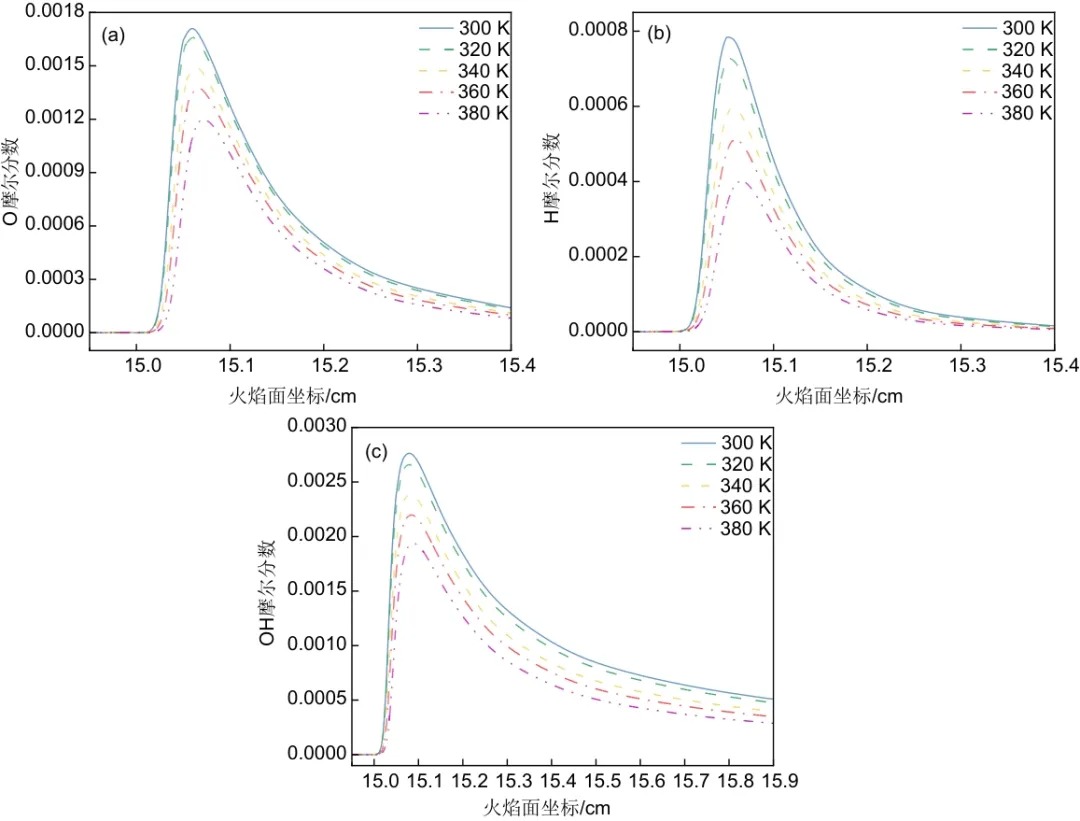
图6 初始温度对 (a) O⋅自由基摩尔分数;(b) H⋅自由基摩尔分数;(c) OH⋅自由基摩尔分数的影响
图7显示了不同初始温度下EMC的爆炸下限工况的OH⋅自由基总生成速率(ROP)以及影响其生成或消耗最大的5个基元反应的生成速率。生成OH的基元反应为H⋅+O2=O⋅+OH⋅、O⋅+H2O=OH⋅+OH⋅、HO2+H⋅=OH⋅+OH⋅和HO2+O⋅=OH⋅+O2,而消耗OH⋅的基元反应为OH⋅+H2=H⋅+H2O。随着温度的升高,各个基元反应的ROP也都在降低。正是由于OH⋅自由基的生成速率不断降低,OH⋅的峰值摩尔分数随着温度的升高而下降,最终引起EMC爆炸下限的变化。
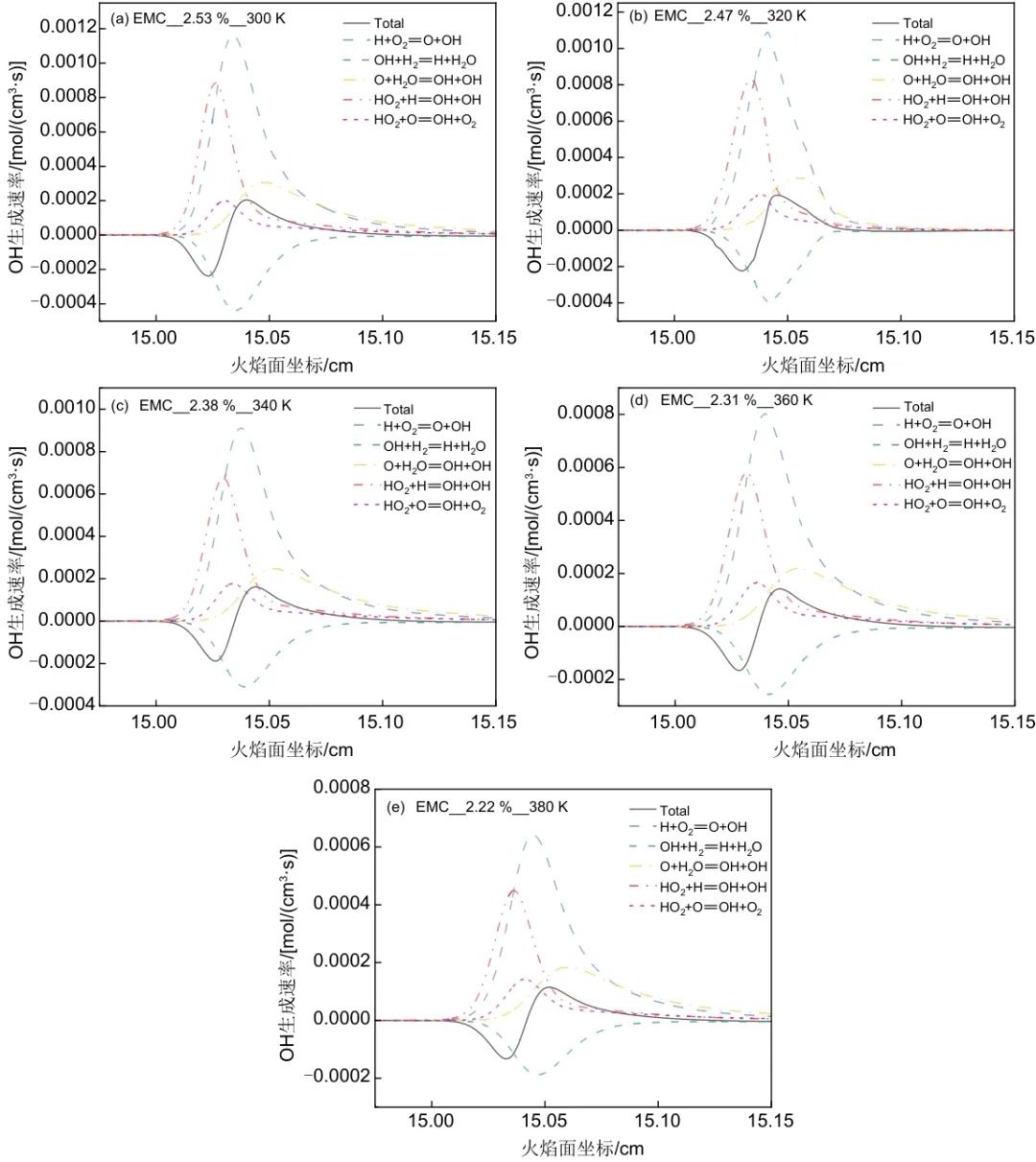
图7 初始温度对OH⋅生成速率的影响
3 结 论
本工作开展了EMC/空气混合气体爆炸实验并进行了数值模拟计算。通过改变当量比以及初始温度条件分析了其对最大爆炸压力Pmax、爆炸下限LFL等爆炸参数的影响,得出的主要结论如下:
(1)EMC/空气混合气体的最大爆炸压力Pmax随着当量比的增加呈先增大后减小的趋势,并且在当量比图片=1.2附近取到最大值,实验值与模拟值分别为753.03 kPa与992.02 kPa。
(2)随着温度的增加,相同容器体积下所含的气体量减少导致最终爆炸能量的减少,使得Pmax呈递减的趋势,而且Pmax与初始温度的倒数1/T0呈线性关系,受限于饱和蒸气压以及爆炸下限的影响,相对于最大绝热爆炸压力Pmax,ad,最大实验爆炸压力Pmax,exp在低当量比工况下与1/T0线性关系并没有那么好;由于存在热损失,在相同工况下,Pmax,exp均小于Pmax,ad。
(3)EMC/空气混合气体的爆炸下限LFL随着T0的升高而降低,并呈线性关系;基于实验数据,对于燃料爆炸下限经典模型的参数进行了修正,得到的预测值与实验值结果很相近;通过反应机理分析得到不同T0对于LFL的影响方式是通过影响OH⋅自由基的生成速率来实现的。
资讯来源:储能科学与技术
免责声明: 本站内容转载自合作媒体、机构或其他网站的信息,转载此文仅出于传递更多信息的目的,但这并不意味着赞同其观点或证实其内容的真实性。本站所有信息仅供参考,不做交易和服务的根据。本站内容如有侵权或其它问题请及时告之,本网将及时修改或删除。凡以任何方式登录本网站或直接、间接使用本网站资料者,视为自愿接受本网站声明的约束。